Description
Arginin langes 3-IGF-1, abgekürzt als IGF-1 LR3 oder LR3-IGF-1, ist ein synthetisches Protein und ein verlängertes Analogon des humanen insulinähnlichen Wachstumsfaktors 1 (IGF-1).
WAS IST IGF-1?
Der insulinähnliche Wachstumsfaktor 1 (IGF-1) ist ein lebenswichtiges Protein, das eine entscheidende Rolle für das Wachstum und die Entwicklung des Menschen spielt. Dieses rekombinante menschliche Protein, das zur Familie der insulinähnlichen Wachstumsfaktoren gehört, besteht aus 70 Aminosäuren und funktioniert ähnlich wie Insulin. Es ist an der Regulierung verschiedener Körperprozesse, einschließlich Wachstum, Entwicklung und Zelldifferenzierung, über endokrine, autokrine und parakrine Wege beteiligt.
Einer der faszinierenden Aspekte von IGF-1 ist sein Zusammenhang mit dem Altern. Untersuchungen legen nahe, dass Mutationen im IGF-1-Gen die Lebensdauer von Labortieren verlängern können, was ihren möglichen Einfluss auf die Langlebigkeit unterstreicht. Bei Kindern ist IGF-1 für die Stimulierung des Zellwachstums und der Zelldifferenzierung unerlässlich, während es bei Erwachsenen weiterhin eine anabole Wirkung ausübt und das Gewebewachstum und den Gewebeerhalt fördert.
IGF-1 agiert in einem komplexen Netzwerk aus Wachstumsfaktoren, Rezeptoren und Bindungsproteinen, die die Zellproliferation, -differenzierung und -apoptose vermitteln. Bei diesen Wachstumsfaktoren handelt es sich um Proteine mit niedrigem Molekulargewicht, die in fast allen Geweben vorkommen und dort die Zellteilung, das Wachstum und die Migration regulieren. In der Haut sind sie beispielsweise entscheidend für die Migration und Entwicklung von Epithelzellen und regen die Zellteilung an.
IGF-1 wird oft als Somatomedin C bezeichnet und dient als Schlüsselmediator der Wirkung des Wachstumshormons (HGH). Es wird hauptsächlich von Hepatozyten der Leber als Reaktion auf die Wachstumshormonstimulation produziert. Die Produktion von IGF-1 durch die Leber wird durch verschiedene Hormone beeinflusst, darunter Sexualsteroide, Schilddrüsenhormone, Glukokortikoide und Insulin. Insulin, Androgene und Östrogene neigen dazu, die IGF-1-Sekretion zu erhöhen, während Glukokortikoide sie hemmen. Diese Wechselwirkung erklärt die Synergie zwischen diesen Hormonen bei Wachstums- und Entwicklungsprozessen und die hemmende Wirkung von Glukokortikoiden auf Wachstum und Pubertät.
Im Laufe des Lebens schwankt der IGF-1-Spiegel, erreicht seinen Höhepunkt im Jugendalter und sinkt im Kindesalter und im Alter. Trotz dieser Unterschiede bleibt IGF-1 ein wichtiges anaboles Hormon. Es wird von verschiedenen Geweben abgesondert, wobei die Leber die Hauptquelle ist, und gibt IGF-1 in den Blutkreislauf ab, um als endokrines Hormon zu wirken. Andere Gewebe, einschließlich Knorpelzellen, sezernieren ebenfalls IGF-1, wo es lokal als parakrines Hormon fungiert.
In den letzten Jahren hat IGF-1 als Dopingwirkstoff in der Sportwelt Aufmerksamkeit erregt und tauchte in zahlreichen aufsehenerregenden Dopingfällen auf. Seine Fähigkeit, Wachstum und Leistung zu steigern, macht es zu einem Stoff, der in Sportgemeinschaften von Interesse und Besorgnis ist.
Was ist der Unterschied zwischen IGF-1 und IGF-1 LR3?
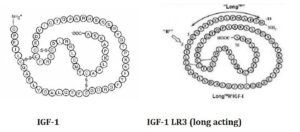
Der insulinähnliche Wachstumsfaktor 1 (IGF-1) und seine erweiterte Variante, IGF-1 LR3, weisen viele Gemeinsamkeiten auf, weisen aber auch deutliche Unterschiede auf, die sich auf ihre Funktionen und Anwendungen auswirken. IGF-1 ist ein natürlich vorkommendes Protein im menschlichen Körper, das für das Zellwachstum, die Entwicklung und die Differenzierung von entscheidender Bedeutung ist. Es besteht aus 70 Aminosäuren und bindet an IGF-1-Rezeptoren, wodurch es verschiedene physiologische Prozesse beeinflusst.
IGF-1 LR3 hingegen ist eine modifizierte Form von IGF-1, die auf eine längere Halbwertszeit und größere Stabilität ausgelegt ist. Diese Variante enthält 13 zusätzliche Aminosäuren am N-Terminus und ersetzt die ursprüngliche dritte Aminosäure, Glutaminsäure, durch ein Arginin. Diese Modifikation verringert die Bindungsaffinität von IGF-1 LR3 zu IGF-bindenden Proteinen, die typischerweise die Verfügbarkeit und Aktivität von IGF-1 regulieren, erheblich. Dadurch bleibt IGF-1 LR3 über einen längeren Zeitraum im Blutkreislauf aktiv und verbessert seine Wirksamkeit bei der Förderung von Wachstum und anabolen Prozessen.
Die verlängerte Halbwertszeit von IGF-1 LR3 macht es sowohl im medizinischen als auch im sportlichen Kontext besonders wertvoll. Aus medizinischer Sicht bietet es potenzielle therapeutische Vorteile für Erkrankungen, die eine längere IGF-1-Aktivität erfordern, wie z. B. Muskelschwunderkrankungen und Wachstumsstörungen. Im Sport und Bodybuilding ist es aufgrund seiner langanhaltenden Wirkung und starken anabolen Wirkung ein gefragtes Mittel zur Verbesserung des Muskelwachstums und der Muskelleistung. Dies wirft jedoch auch Bedenken hinsichtlich seines Missbrauchs und seiner ethischen Implikationen im Leistungssport auf.
Zusammenfassend lässt sich sagen, dass sowohl IGF-1 als auch IGF-1 LR3 eine wichtige Rolle bei Wachstum und Entwicklung spielen, der Hauptunterschied jedoch in der manipulierten Struktur von IGF-1 LR3 liegt, die eine längere Halbwertszeit und größere Kraft verleiht. Diese Unterscheidung erweitert nicht nur die potenziellen therapeutischen Anwendungen, sondern unterstreicht auch die Notwendigkeit einer sorgfältigen Regulierung, um Missbrauch im Sportumfeld zu verhindern.
HAUPTEFFEKTE
IGF-1 ist ein äußerst wirksames Anabolikum, das in Kombination mit anabolen Steroiden zu einer spürbaren Steigerung der Muskelmasse führt. Gleichzeitig verfügt IGF-1 über viele weitere nützliche Eigenschaften, die zusammen den maximalen Wachstumsschub bewirken. IGF-1 ist ein Produkt, das Ihre Ergebnisse verbessern kann, wenn andere Methoden keine signifikante Wirkung mehr erzielen.
Anabole Wirkung
- Erhöhte Muskelmasse (verschiedene Belichtungsmodi)
- Muskelhyperplasie (einzigartige Eigenschaft, die Anzahl der Muskelzellen zu erhöhen)
- Beschleunigte Proteinsynthese
- Regeneration des Sehnengewebes (erhöht die Kollagensynthese)
- Es hat eine reparierende Wirkung auf das Knorpelgewebe
- Erhöht die Wirksamkeit von anabolen Steroiden (erhöht die Anzahl der Androgenrezeptoren)
- Stellt Knochen- und Knorpelgewebe wieder her und stärkt es
Unterstützung des Herz-Kreislauf-Systems
- Verbessert das Herzzeitvolumen, das systolische Volumen, die Kontraktilität und die Ejektionsfraktion.
- Stimuliert die Kontraktilität und den Umbau des Gewebes beim Menschen, um die Herzfunktion nach einem Myokardinfarkt zu verbessern.
- Verbessert das Lipidprofil
- Reduziert den Insulinspiegel, erhöht die Insulinsensitivität und fördert den Glukosestoffwechsel
- Reduzieren Sie das Gesamtrisiko kardiovaskulärer Komplikationen
- Hilft bei der Bekämpfung entzündlicher Prozesse
Nervengewebe
- Erhöht den Transport von Glukose in das Nervengewebe
- Schützt Neuronen bei niedrigem Glukosespiegel und verhindert die Zellzerstörung.
- Sie spielen eine wichtige Rolle bei der Wiederherstellung von Neuronen und Nervengewebe im Allgemeinen
Andere Effekte
- Regulieren Sie die Expression von Genen, die die Lebenserwartung erhöhen.
- Beschleunigt die Hautregeneration und beugt Hautalterung vor
- Verbesserte Immunität
Wirkungsmechanismus
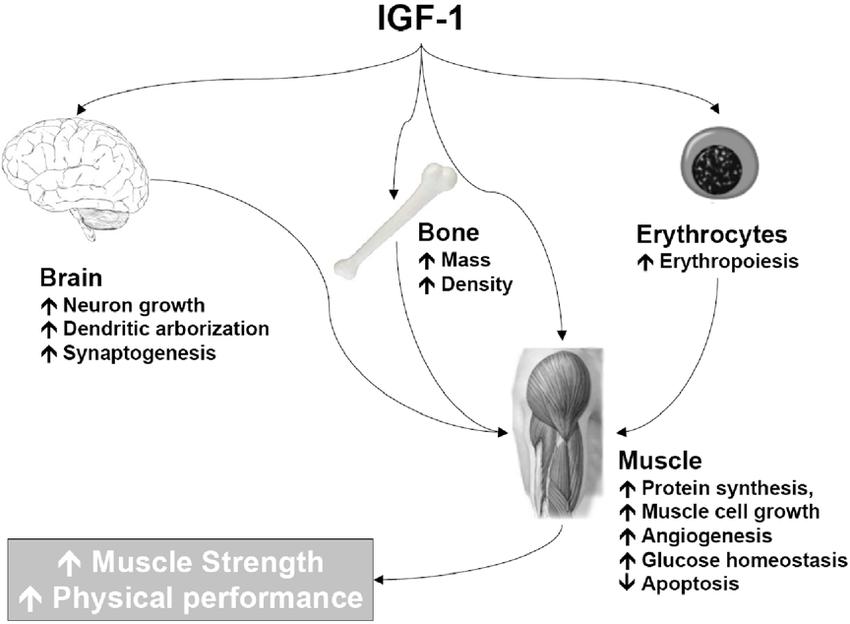
Der insulinähnliche Wachstumsfaktor 1 (IGF-1) ist ein lebenswichtiges Protein, das eine entscheidende Rolle bei der Regeneration und Reparatur verschiedener Gewebe im menschlichen Körper spielt, darunter Knochen, Muskeln, Haut und Knorpel. Wenn IGF-1 mit Knochen- und Knorpelgewebe interagiert, bindet es an spezifische Rezeptoren auf Osteoblasten und Chondroblasten, Zellen, die für das Wachstum und die Reparatur von Knochen und Knorpel verantwortlich sind. Diese Bindung regt die Stoffwechselaktivität dieser Zellen an, was zu einer beschleunigten Heilung von Frakturen und anderen Knochenverletzungen führt. IGF-1 reduziert auch Entzündungen in geschädigten Bereichen und steigert so die Aktivität von Zellen, die an der Gewebeerneuerung beteiligt sind (Yakar et al., 2019).
Darüber hinaus gehen die metabolischen Wirkungen von IGF-1 über Wachstum und Reparatur hinaus. Es spielt eine wichtige Rolle bei der Nährstoffsignalisierung und koordiniert den Stoffwechsel von Proteinen, Fetten und Kohlenhydraten in verschiedenen Zelltypen. Dies wird durch die Stimulation von IGF-1-Rezeptoren erreicht, die den Zellen die Verfügbarkeit von Nährstoffen signalisieren. Diese Koordination trägt dazu bei, dass die Zellen die Nährstoffe erhalten, die sie für Wachstum und Erhaltung benötigen. Wie Insulin wird IGF-1 durch den Ernährungszustand reguliert und ist an der Glukosehomöostase beteiligt. Es senkt den Blutzuckerspiegel, indem es die Glukoseaufnahme in die Zellen erhöht und die Insulinsekretion verringert, was die Insulinsensitivität erhöht (Samani et al., 2007).
Zusätzlich zu seiner Rolle im Stoffwechsel beeinflusst IGF-1 auch den Proteinstoffwechsel und die Lipolyse. Es wirkt synergistisch mit Wachstumshormon (GH), um den Fettabbau zu verbessern und die Ketogenese zu fördern. Diese Synergie zwischen IGF-1 und GH ist für die Aufrechterhaltung des Energiegleichgewichts und die Unterstützung von Wachstumsprozessen unerlässlich. Studien haben gezeigt, dass niedrige IGF-1-Spiegel häufig mit dem metabolischen Syndrom verbunden sind, einer Reihe von Erkrankungen, die das Risiko für Herzerkrankungen, Schlaganfall und Diabetes erhöhen. Dies unterstreicht die Bedeutung von IGF-1 für die Aufrechterhaltung der allgemeinen Stoffwechselgesundheit (Clemmons, 2004).
Auswirkungen auf die Muskeln
IGF-1 hat einen tiefgreifenden Einfluss auf das Muskelgewebe und fördert das Muskelwachstum und die Muskelreparatur. Dies wird vor allem durch die Stimulation von Satellitenzellen erreicht, bei denen es sich um Stammzellen handelt, die sich im Muskelgewebe befinden. Wenn Muskelgewebe geschädigt wird, aktiviert IGF-1 diese Satellitenzellen, wodurch sie sich vermehren und in neue Muskelzellen differenzieren. Dieser Prozess repariert nicht nur beschädigte Muskelfasern, sondern führt auch zu einer Zunahme der Muskelmasse. Die Fähigkeit von IGF-1, die Muskelregeneration zu verbessern, macht es zu einer Schlüsselbehandlung bei Erkrankungen, die mit Muskelatrophie einhergehen, wie z. B. Muskeldystrophie (Ahmad et al., 2020).
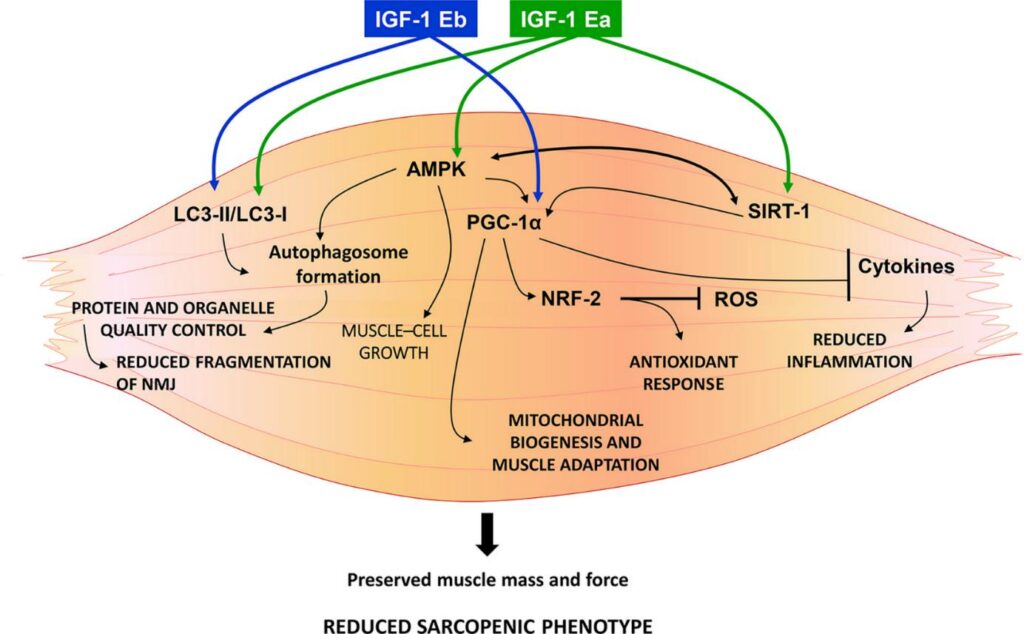
Die molekularen Mechanismen, durch die IGF-1 das Muskelwachstum stimuliert, umfassen verschiedene Signalwege. Einer der Hauptwege ist der PI-3-Kinase-Weg, der zur Aktivierung der Proteinkinase B (AKT) führt. AKT fördert dann die Proteinsynthese, indem es den mTOR-Signalweg aktiviert, einen entscheidenden Regulator des Zellwachstums und der Proteinsynthese. Darüber hinaus verbessert IGF-1 den Transport von Aminosäuren in die Muskelzellen und stellt so die für die Proteinsynthese notwendigen Elemente bereit. IGF-1 hemmt auch den Proteinabbau, indem es die Expression von Genen, die an der Muskelatrophie beteiligt sind, wie MuRF1 und MAFbx, herunterreguliert (Lai et al., 2004).
Zusätzlich zu seiner anabolen Wirkung hat IGF-1 auch antikatabole Eigenschaften. Wirkt der Wirkung entzündlicher Zytokine entgegen, die den Muskelabbau fördern. Durch die Hemmung dieser katabolen Stoffwechselwege trägt IGF-1 dazu bei, Muskelmasse und -funktion zu erhalten, selbst unter Stress- oder Krankheitsbedingungen. Diese doppelte Rolle der Förderung des Muskelwachstums und der Verhinderung des Muskelabbaus macht IGF-1 zu einem wesentlichen Faktor bei der Aufrechterhaltung der Muskelgesundheit und -funktion (Lai et al., 2004).
Auswirkungen auf das Sehnengewebe
Sehnenverletzungen heilen bekanntermaßen nur langsam, was häufig zu fibrovaskulären Narben führt, die die mechanischen Eigenschaften der Sehnen beeinträchtigen und das Risiko einer erneuten Verletzung erhöhen. Es wurde gezeigt, dass IGF-1 die Heilung der Sehnen deutlich verbessert, indem es die Zellproliferation, die DNA-Synthese und die Matrixproduktion fördert, insbesondere Kollagen I, den Hauptbestandteil des Sehnengewebes. Dies macht IGF-1 zu einem wirksamen anabolen Wirkstoff zur Verbesserung der Sehnenreparatur und -funktion (Miescher et al., 2023).
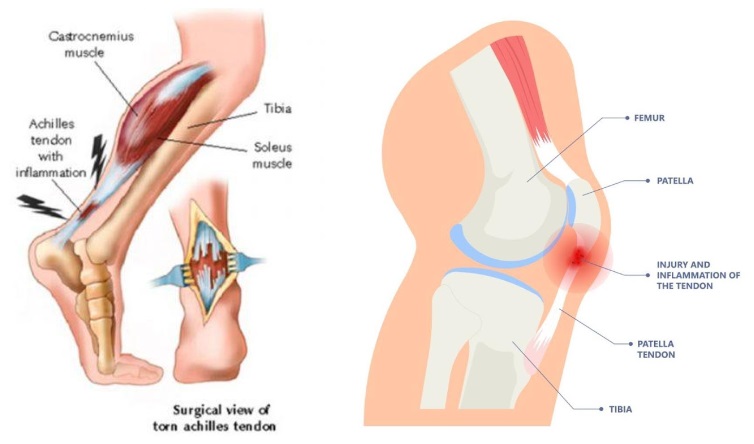
Der Mechanismus, durch den IGF-1 die Sehnenheilung fördert, umfasst mehrere zelluläre Prozesse. Bei Anwendung auf Tenozytenkulturen – Zellen, aus denen Sehnen bestehen – stimuliert IGF-1 diese Zellen zur Proliferation und zur Produktion weiterer extrazellulärer Matrixkomponenten, einschließlich Kollagen. Diese erhöhte Matrixproduktion bietet die für die Sehnenreparatur erforderliche strukturelle Unterstützung. Darüber hinaus reduziert IGF-1 nachweislich Entzündungen in der verletzten Sehne und unterstützt den Heilungsprozess weiter, indem es ein günstigeres Umfeld für die Geweberegeneration schafft (Disser et al., 2019).
In präklinischen Tiermodellen und bei menschlichen Patienten hat IGF-1 seine Wirksamkeit bei der Verbesserung der Sehnenheilungsergebnisse gezeigt. Studien haben beispielsweise gezeigt, dass die Anwendung von IGF-1 auf verletzte Sehnen in Tiermodellen den Heilungsprozess beschleunigt, Narbenbildung reduziert und die mechanischen Eigenschaften geheilter Sehnen verbessert. Diese Ergebnisse legen nahe, dass IGF-1 ein wertvolles therapeutisches Mittel zur Behandlung von Sehnenverletzungen im klinischen Umfeld sein könnte. (Doessing et al., 2010)
Auswirkungen auf Knorpelgewebe
IGF-1 spielt eine entscheidende Rolle bei der Erhaltung und Reparatur von Knorpelgewebe, das für die Gesundheit und Funktion der Gelenke unerlässlich ist. Knorpel ist ein starkes, glattes, elastisches Gewebe, das die Enden langer Knochen an den Gelenken bedeckt und schützt. Es dient auch als Polster zwischen den Knochen und ermöglicht eine reibungslose, schmerzfreie Bewegung. IGF-1 reguliert den Knorpelstoffwechsel, indem es anabole Prozesse fördert und katabole Prozesse hemmt, wodurch die Integrität und Funktion des Knorpels erhalten bleibt (Wen et al., 2021).
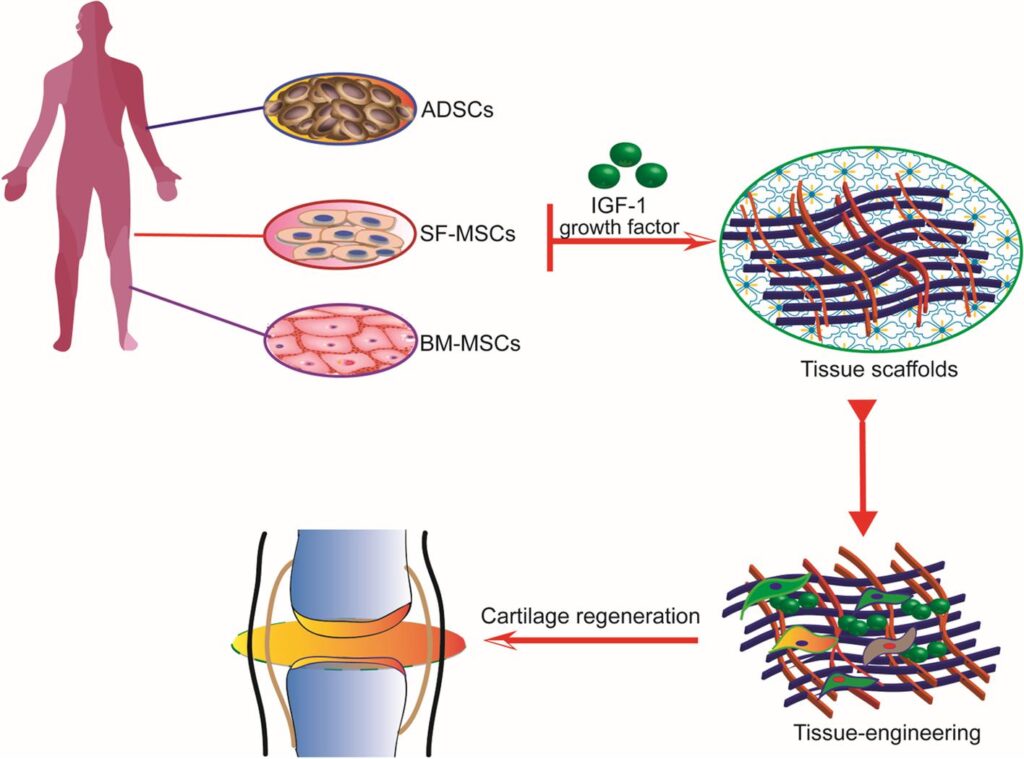
Die primären Zellen, die für die Erhaltung des Knorpels verantwortlich sind, sind Chondrozyten. IGF-1 stimuliert diese Zellen zur Produktion extrazellulärer Matrixkomponenten wie Kollagen und Proteoglykane, die für die Struktur und Funktion des Knorpels unerlässlich sind. IGF-1 fördert nicht nur die Matrixsynthese, sondern hemmt auch die Aktivität knorpelzerstörender Enzyme wie Matrix-Metalloproteinasen (MMPs). Diese doppelte Wirkung der Förderung anaboler Prozesse und der Hemmung kataboler Prozesse trägt dazu bei, Knorpelgewebe zu erhalten und dessen Degeneration zu verhindern (Vedadghavami, 2022).
Studien haben gezeigt, dass IGF-1 das Fortschreiten von Arthrose verlangsamen kann, einer degenerativen Gelenkerkrankung, die durch den Abbau von Knorpel gekennzeichnet ist. Die wirksame Abgabe von IGF-1 an geschädigten Knorpel ist für seine therapeutische Wirkung von entscheidender Bedeutung. Techniken wie intraartikuläre Injektionen und lokalisierte Abgabesysteme werden untersucht, um sicherzustellen, dass IGF-1 das Zielgewebe in ausreichenden Konzentrationen erreicht. Tierstudien haben gezeigt, dass die kontinuierliche Verabreichung von IGF-1 den Knorpelabbau verhindern und die Reparatur fördern kann, was sein Potenzial zur Behandlung von Arthrose unterstreicht (Wen et al., 2021).
Knochengewebe
IGF-1 beeinflusst den Knochenstoffwechsel erheblich, indem es sowohl die Knochenresorption als auch die Knochenbildung fördert. Diese doppelte Wirkung ist von grundlegender Bedeutung für den Knochenumbau, einen kontinuierlichen Prozess, bei dem altes Knochengewebe durch neues Knochengewebe ersetzt wird. IGF-1 regt Osteoblasten, die für die Knochenbildung verantwortlichen Zellen, an, neue Knochenmatrix zu produzieren. Es fördert auch die Aktivität von Osteoklasten, den Zellen, die für die Knochenresorption verantwortlich sind, um alten oder beschädigten Knochen zu entfernen und so den Ersatzprozess zu erleichtern (Canalis, 2009).
Die Auswirkungen von IGF-1 auf die Knochengesundheit sind besonders deutlich bei Erkrankungen mit Knochenbrüchen und Osteoporose. Studien haben gezeigt, dass die Verabreichung von IGF-1 an Frakturpatienten die Knochenheilung beschleunigen und die klinischen Ergebnisse verbessern kann. Beispielsweise wurde festgestellt, dass die IGF-1-Behandlung die Knochenmineraldichte erhöht und die strukturellen Eigenschaften des geheilten Knochens verbessert, wodurch er stärker und weniger anfällig für erneute Verletzungen wird (Locatelli & Bianchi., 2014).
Zusätzlich zu seinen direkten Auswirkungen auf Knochenzellen beeinflusst IGF-1 auch die Knochengesundheit, indem es mit anderen Hormonen wie Parathormon (PTH) und Vitamin D interagiert. Diese Interaktionen tragen zur Regulierung der Kalziumhomöostase bei und stellen sicher, dass die Knochen ausreichend Nährstoffe für das Wachstum erhalten und Wachstum. reparieren. Durch die Modulation dieser hormonellen Wege spielt IGF-1 eine entscheidende Rolle bei der Aufrechterhaltung der Knochengesundheit und der Vorbeugung von Krankheiten wie Osteoporose (Canalis, 2010).
IGF-1 und Glukosestoffwechsel
IGF-1 hat erhebliche Auswirkungen auf den Glukosestoffwechsel, insbesondere durch die Verbesserung der Insulinsensitivität und die Regulierung des Blutzuckerspiegels. Stimuliert den Glukosetransport in Muskelzellen über IGF-1-Rezeptoren oder Hybrid-Insulin/IGF-1-Rezeptoren. Durch die Erhöhung der Glukoseaufnahme in Muskelzellen trägt IGF-1 zur Senkung des Blutzuckerspiegels bei und verringert so den Bedarf an Insulinsekretion (Clemmons, 2004).
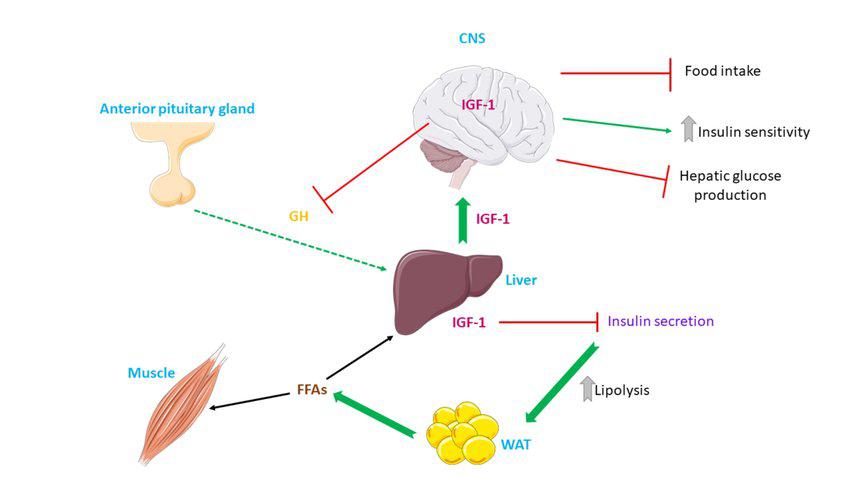
Beschreibung der durch IGF-1 hervorgerufenen Stoffwechselvorgänge. IGF-1 wird hauptsächlich von der Leber freigesetzt und verbessert die Insulinsensitivität, indem es die Insulinsekretion unterdrückt, was wiederum zu einer erhöhten Lipolyse im Fettgewebe führt und die NEFA-Nutzung in Muskeln und Leber fördert. Verwendete Abkürzungen: ZNS: zentrales Nervensystem; GH: Wachstumshormon; IGF-1: Insulin-Wachstumsfaktor-1; FFA: freie Fettsäuren; WAS: weißes Fettgewebe
In Tiermodellen wurde gezeigt, dass hohe Konzentrationen an freiem IGF-1 die Gluconeogenese hemmen, den Prozess, bei dem Glucose aus Nicht-Kohlenhydratquellen in der Leber produziert wird. Diese Hemmung trägt zur Senkung des Blutzuckerspiegels bei und verbessert die allgemeine Glukosehomöostase. Darüber hinaus haben Studien gezeigt, dass die Entfernung des Insulinrezeptors bei Mäusen den Blutzuckerspiegel als Reaktion auf IGF-1 senkt, was darauf hindeutet, dass IGF-1 die Rolle von Insulin im Glukosestoffwechsel in gewissem Maße kompensieren kann (Clemmons, 2004).
Klinische Studien haben auch die Bedeutung von IGF-1 für die Aufrechterhaltung des Glukosestoffwechsels hervorgehoben. Untersuchungen haben beispielsweise gezeigt, dass niedrige IGF-1-Serumspiegel mit einer beeinträchtigten Glukosetoleranz und einem erhöhten Risiko für Typ-2-Diabetes verbunden sind. Umgekehrt sind höhere IGF-1-Spiegel mit einer verbesserten Insulinsensitivität und einem niedrigeren Blutzuckerspiegel verbunden. Diese Ergebnisse legen nahe, dass IGF-1 eine entscheidende Rolle bei der Vorbeugung von Stoffwechselstörungen und der Aufrechterhaltung der Glukosehomöostase spielt (Rajpathak et al., 2014).
IGF-1 und Altern
Der IGF-1-Signalweg ist in verschiedenen Arten, von Wirbellosen bis hin zu Säugetieren, hoch konserviert. Dieser Weg ist entscheidend für die Regulierung von Wachstum, Entwicklung und Lebensdauer. Bei Säugetieren umfasst der IGF-1-Signalweg ein komplexes Netzwerk von Signalen, die zelluläre Prozesse wie Wachstum, Stoffwechsel und Alterung beeinflussen. IGF-1 übt seine Wirkung über den IGF-1-Rezeptor aus, der eine Kaskade intrazellulärer Signalwege aktiviert, die das Zellwachstum und das Überleben fördern (Kenyon, 2010).

GH/IGF-1-Achsenfaktoren, von denen bekannt ist, dass sie das Altern beeinflussen. Die embryonal exprimierten Gene PROP1 (kodiert für PROP-1) und POU1F1 (kodiert für PIT-1) sind an der Entwicklung der Hypophyse beteiligt, einschließlich der Differenzierung somatotropher Zellen der Hypophyse.
Wenn bei Wirbellosen ein Insulin/IGF-1-Weg existiert, ist dieser Weg bei höheren Wirbeltieren, einschließlich Säugetieren, in zwei Teile unterteilt. Diese beiden Wege haben überlappende Funktionen, aber Insulin ist hauptsächlich an der Regulierung des Stoffwechsels beteiligt, und der Wachstumshormon/IGF-1-Weg spielt eine wichtige Rolle bei den Prozessen des Wachstums, der Entwicklung und möglicherweise der Lebenserwartung. Es waren die IGF-1-Kaskadengene, die als erste „Alterungsgene“ entdeckt wurden, also Gene, deren Schädigung zu einer Erhöhung der Lebenserwartung führte.
Beim Menschen wurden Veränderungen der IGF-1-Spiegel und der IGF-1-Signalübertragung mit altersbedingten Krankheiten in Verbindung gebracht. Niedrige IGF-1-Spiegel sind häufig mit einem erhöhten Risiko für Herz-Kreislauf-Erkrankungen, Diabetes und neurodegenerative Erkrankungen verbunden. Umgekehrt sind höhere IGF-1-Spiegel mit besseren Gesundheitsergebnissen und einem geringeren Risiko für diese Erkrankungen verbunden. Diese Ergebnisse unterstreichen die Bedeutung von IGF-1 für die Förderung eines gesunden Alterns und die Vorbeugung altersbedingter Krankheiten (Kenyon, 2010).
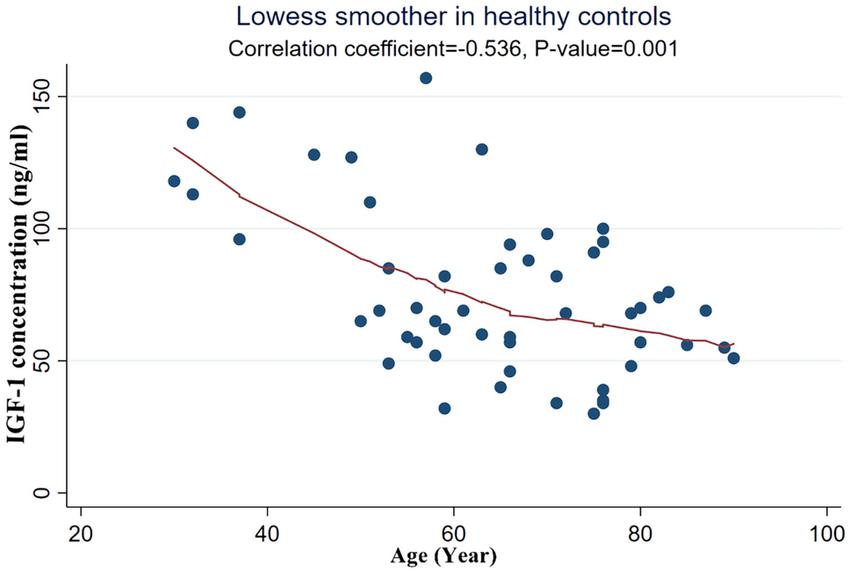
Auswirkungen auf die Haut
IGF-1 spielt eine entscheidende Rolle bei der Erhaltung der Hautgesundheit und der Förderung der Wundheilung. Es wirkt als Regulator und Stimulator der Zellteilung im Epithelgewebe und fördert das Wachstum und den Stoffwechsel von Zellen in den tieferen Hautschichten. Dies führt zu einer beschleunigten Kollagensynthese und einer schnelleren Heilung sowohl oberflächlicher als auch tieferer Wunden. IGF-1 spielt auch eine Schlüsselrolle bei der Aufrechterhaltung der epidermalen Homöostase und trägt dazu bei, der Hautalterung vorzubeugen und ein jugendliches Aussehen zu bewahren (Tavakkol et al., 1999).
Der Mechanismus, durch den IGF-1 die Hautgesundheit fördert, umfasst mehrere zelluläre Prozesse. Wenn die Haut geschädigt ist, stimuliert IGF-1 die Proliferation von Keratinozyten, den primären Zellen der Epidermis, und Fibroblasten, den Zellen, die für die Produktion von Kollagen und anderen Bestandteilen der extrazellulären Matrix verantwortlich sind. Diese erhöhte Zellproliferation und Matrixproduktion hilft, geschädigte Haut zu reparieren und ihre strukturelle Integrität wiederherzustellen. Darüber hinaus verstärkt IGF-1 die Migration dieser Zellen zur Wundstelle und beschleunigt so den Heilungsprozess weiter (Zhang et al., 2024).

Der Einfluss des Alterns auf die Expression des insulinähnlichen Wachstumsfaktors 1 (IGF-1) in der Haut und seine Rolle bei der durch Ultraviolett-B (UVB) induzierten Karzinogenese.
Studien haben gezeigt, dass IGF-1 die Haut auch vor den Auswirkungen des Alterns schützen kann. Durch die Förderung der Kollagensynthese und die Verringerung des Abbaus von Kollagenfasern trägt IGF-1 zur Aufrechterhaltung der Elastizität und Festigkeit der Haut bei. Dieser Anti-Aging-Effekt ist besonders wichtig, um der Faltenbildung vorzubeugen und einen glatten, jugendlichen Teint zu erhalten. Darüber hinaus wurde festgestellt, dass IGF-1 Hautentzündungen reduziert, was dazu beitragen kann, chronischen Hauterkrankungen vorzubeugen und die allgemeine Hautgesundheit zu verbessern (Muraguchi et al., 2019).
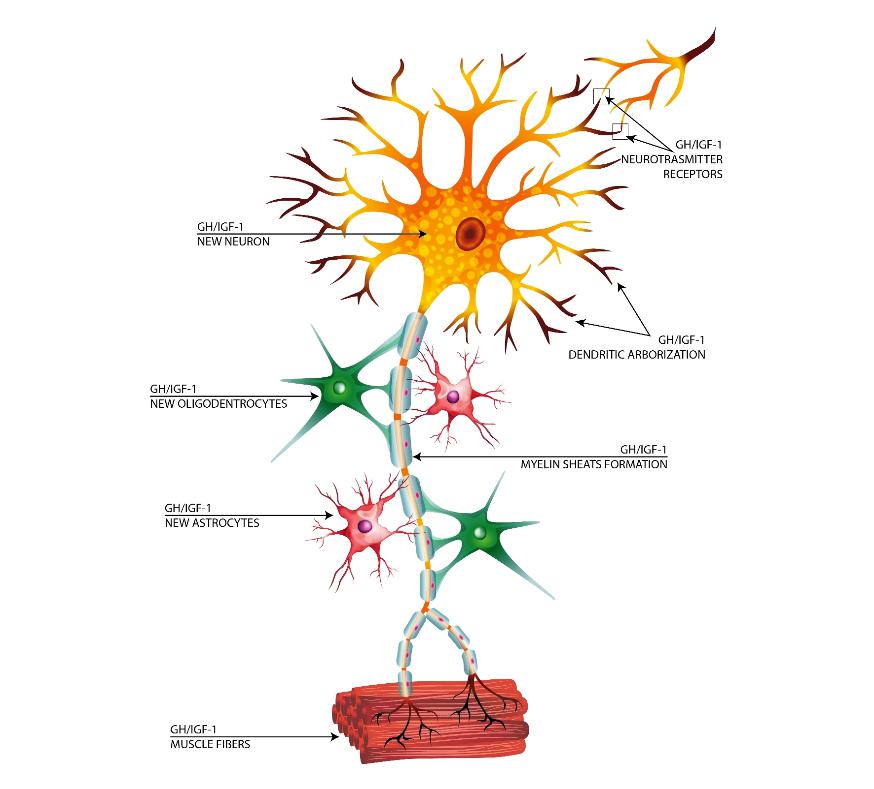
Auswirkungen auf das Nervengewebe
IGF-1 hat erhebliche neuroprotektive Wirkungen und verbessert das Überleben und die Funktion von Neuronen. Es erhöht den Transport von Glukose in die Neuronen und versorgt sie mit der Energie, die sie für eine korrekte Funktion benötigen. Dies ist besonders wichtig bei Bedingungen mit niedrigem Glukosespiegel, wo IGF-1 hilft, neuronale Schäden und Zelltod zu verhindern. Darüber hinaus stimuliert IGF-1 die neuronale RNA-Synthese und fördert die Bildung von Axonen, den langen Fortsätzen von Neuronen, die Nervensignale übertragen (Dyer et al., 2016).
Im Nervensystem fördert IGF-1 auch die Proliferation von Gliazellen, die den Neuronen Unterstützung und Schutz bieten. Zu diesen Gliazellen gehören Astrozyten, Oligodendrozyten und Mikroglia, die jeweils eine entscheidende Rolle bei der Aufrechterhaltung der Gesundheit und Funktion des Nervensystems spielen. Durch die Förderung der Proliferation und Funktion dieser Zellen trägt IGF-1 dazu bei, eine unterstützende Umgebung für Neuronen zu schaffen und deren Wachstum, Reparatur und Überleben zu erleichtern (Carson et al., 1993).
Die neuroprotektiven Wirkungen von IGF-1 sind insbesondere bei neurodegenerativen Erkrankungen wie Alzheimer und Parkinson relevant. Untersuchungen haben gezeigt, dass IGF-1 die Bildung toxischer Proteine wie Beta-Amyloid-Plaques bei der Alzheimer-Krankheit reduzieren und die Clearance dieser Proteine aus dem Gehirn verbessern kann. Dies trägt dazu bei, Neuronen vor Schäden zu schützen und unterstützt die kognitive Funktion. Darüber hinaus wurde festgestellt, dass IGF-1 die Regeneration geschädigter Neuronen fördert und potenzielle therapeutische Vorteile bei neurodegenerativen Erkrankungen bietet (Dyer et al., 2016).
Auswirkungen auf das Herz-Kreislauf-System
IGF-1 spielt eine besondere Rolle für die Herz-Kreislauf-Gesundheit, indem es die Entwicklung und Funktion des Herzens und der Blutgefäße fördert. Es verbessert die Herzleistung, das Schlagvolumen, die Kontraktilität und die Ejektionsfraktion, allesamt entscheidend für die Aufrechterhaltung einer effizienten Herzfunktion. IGF-1 stimuliert auch den Umbau des Herzgewebes und hilft so, Schäden nach einem Myokardinfarkt zu reparieren und die allgemeine Herzgesundheit zu verbessern (Macvanin et al., 2023).
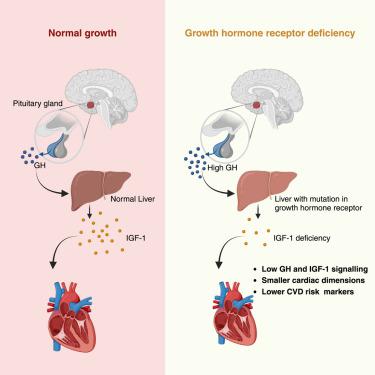
Die kardiovaskulären Wirkungen von IGF-1 werden durch mehrere Mechanismen vermittelt. Erstens fördert IGF-1 die Proliferation und das Überleben von Kardiomyozyten, den Muskelzellen des Herzens. Dies trägt zur Aufrechterhaltung der strukturellen Integrität und der kontraktilen Funktion des Herzens bei. Zweitens stimuliert IGF-1 die Angiogenese, die Bildung neuer Blutgefäße, was den Blutfluss und die Sauerstoffversorgung des Herzens und anderer Gewebe verbessert. Drittens hat IGF-1 antiapoptotische und entzündungshemmende Wirkungen und reduziert Zelltod und Entzündungen im Herz-Kreislauf-System (De Giorgi et al., 2022).
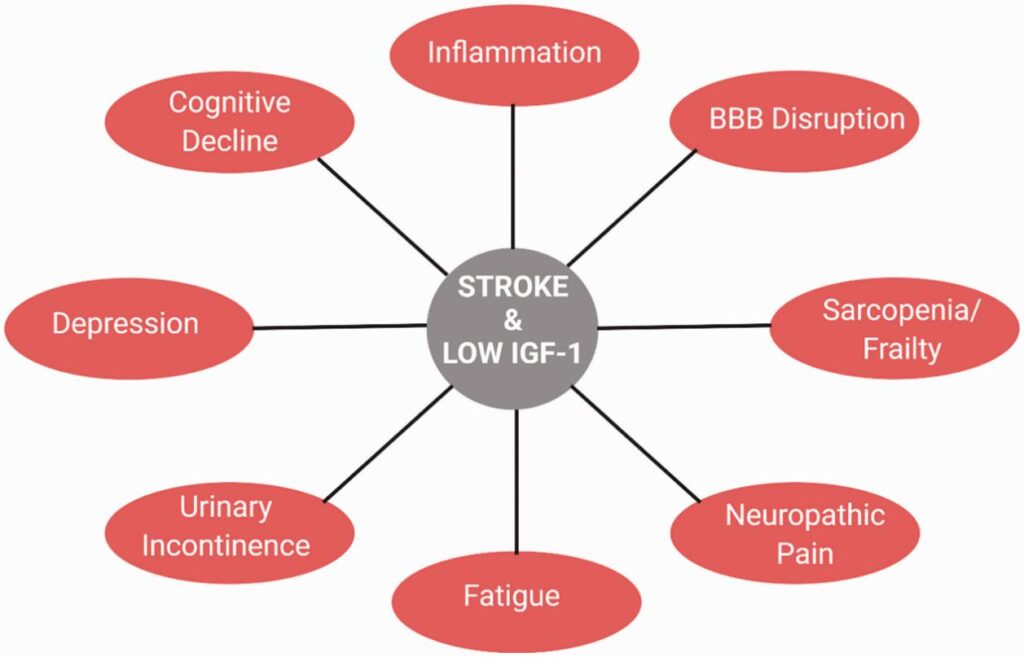
Klinische Studien haben gezeigt, dass niedrige IGF-1-Spiegel mit einem erhöhten Risiko für Herz-Kreislauf-Erkrankungen, einschließlich koronarer Herzkrankheit und Schlaganfall, verbunden sind. Umgekehrt sind höhere IGF-1-Spiegel mit einer besseren Herz-Kreislauf-Gesundheit und einem geringeren Risiko für diese Erkrankungen verbunden. Beispielsweise fanden sie in einer prospektiven Patientenkohortenstudie heraus, dass Teilnehmer mit höheren IGF-1-Werten ein um 55 % geringeres relatives Risiko für einen Myokardinfarkt hatten als Teilnehmer mit niedrigeren Werten (Macvanin et al., 2023).
Auswirkungen auf die Immunität
IGF-1 hat einen erheblichen Einfluss auf das Immunsystem und verbessert die Funktion und Proliferation verschiedener Immunzellen. Es erhöht die Populationen von T-Lymphozyten, B-Lymphozyten und natürlichen Killerzellen, die alle eine entscheidende Rolle bei der Abwehr des Körpers gegen Infektionen und Krankheiten spielen. IGF-1 steigert auch die Aktivität von T-Lymphozyten, die für die zellvermittelte Immunität und die Zerstörung infizierter oder krebsartiger Zellen unerlässlich sind (Alpdogan et al., 2003).
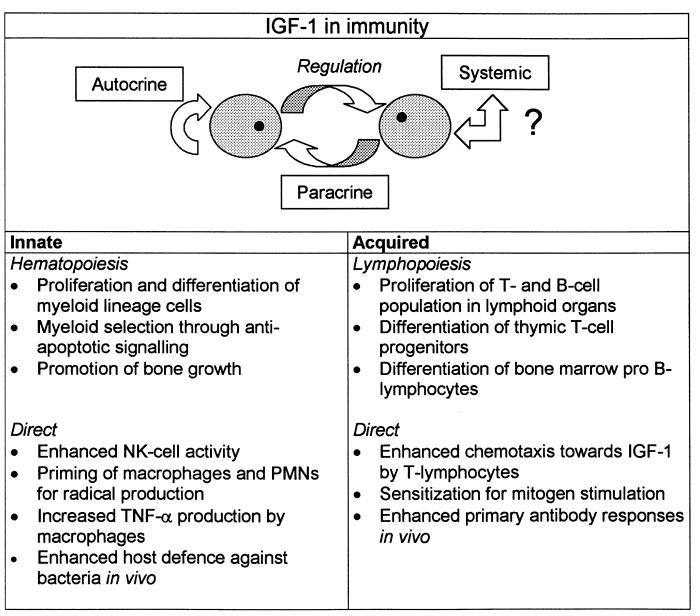
Die immunstärkende Wirkung von IGF-1 wird durch mehrere Mechanismen vermittelt. IGF-1 stimuliert die Proliferation von Immunzellen, indem es an seine Rezeptoren auf deren Oberfläche bindet, was zu einer erhöhten Zellteilung und einem erhöhten Zellwachstum führt. Dies ist besonders wichtig für die Ausbreitung von Immunzellpopulationen als Reaktion auf Infektionen oder immunologische Herausforderungen. Darüber hinaus verbessert IGF-1 die Funktion dieser Zellen, indem es ihre Aktivierung fördert und ihre Fähigkeit erhöht, auf Krankheitserreger zu reagieren (Dyer et al., 2016).
Untersuchungen haben gezeigt, dass IGF-1 Immunzellen auch vor Apoptose oder dem programmierten Zelltod schützen kann, was für die Aufrechterhaltung einer robusten Immunantwort von entscheidender Bedeutung ist. Studien haben beispielsweise gezeigt, dass IGF-1 die Apoptose von Makrophagen und Neutrophilen hemmen kann, zwei Schlüsseltypen von Immunzellen, die an der ersten Reaktion des Körpers auf Infektionen beteiligt sind. Durch die Erhaltung der Vitalität dieser Zellen trägt IGF-1 dazu bei, eine wirksame und unterstützte Immunantwort zu gewährleisten (Alpdogan et al., 2003).
Anwendung von IGF-1 LR3
Nigf-1 LR3 ist oft die Geheimwaffe professioneller Bodybuilder. Es ist die Verwendung dieses Produkts, das den nächsten Schritt zum Fortschritt nach anabolen Steroiden und Wachstumshormonen darstellt, die bei Ped-Liebhabern seit langem an Beliebtheit gewonnen haben.
Nilprodukt IGF-1 LR3 hat eine sehr breite Wirkung und kann sowohl zur Fettverbrennung als auch zur Beschleunigung der Heilung von Läsionen und zur Stärkung des Gelenk-Rechts-Apparats, zur Erhöhung der Muskelmasse und zur Beschleunigung der Erholung nach der Anstrengung verwendet werden, da die Substanz auch die Erholung beeinflusst des Nervensystems. Die IGF-1 LR3-Software verfügt über ein reichhaltiges Spektrum an Eigenschaften, die für viele Zwecke geeignet sind und eine hervorragende Ergänzung zu jedem Ihrer Kurse sein werden, egal ob es sich um einen Muskelaufbau oder ein präagonistisches Training handelt.
Dosierung: </ h2>
Anfänger: 20-40 µg pro Tag
Mittelstufe: 40–60 µg pro Tag
Fortgeschritten: 60–100 µg pro Tag
Nin-Genre, 4-6 Wochen, gefolgt von einer gleich langen Pause, um eine Desensibilisierung zu vermeiden.
Verwaltungsprogramm:
Häufigkeit: tägliche Injektionen
Zeitpunkt: wird morgens oder nach dem Training verabreicht, um die Absorption und Wirksamkeit zu maximieren.
Injektionsstelle: subkutane oder intramuskuläre Injektionen, rotierende Stellen, um Schäden vorzubeugen.
Beispiel
Überdosierung
Eine Überdosierung kann die oben aufgeführten Nebenwirkungen verursachen. Sehr häufig handelt es sich um eine Hypoglykämie, also einen Abfall des Zuckers unter den Schwellenwert von 3,5 mmol/l. In diesem Fall ist es notwendig, eine bestimmte Menge kohlenhydrathaltiger Lebensmittel zu sich zu nehmen, bis sich der Zustand stabilisiert.
Verwaltungsmethoden
Intamuskuläre oder subkutane Injektionen mit Insulinspritzen.
Erkennung bei Anti-Doping-Tests
NSE unterbricht die Einnahme des Medikaments drei Tage vor dem Test, niemand wird die Substanz im Blut nachweisen können.
Blutuntersuchungen auf IGF-1 (Somatomedin C)
Normalerweise wird die Bioaktivität des Wachstumshormons im menschlichen Körper durch Analyse des Somatomedin C einige Wochen nach der ersten Injektion bestimmt. Auf diese Weise können wir die Wirksamkeit des Wachstumshormons auf den Körper bestimmen, da die meisten seiner Wirkungen über das IGF-1-Protein erfolgen. Dies liegt daran, dass das Wachstumshormon die Freisetzung von IGF-1 verursacht. Das Wachstumshormon bewirkt aber auch die Freisetzung von IGFBP, einem Protein, das IGF-1 bindet. Der Komplex IGF-1: IGFBP zirkuliert im Blut. In den Blutuntersuchungen nach mehrwöchiger Verabreichung des exogenen Wachstumshormons können wir die Testergebnisse für Homatomodin C sehen – 500 ng/ml oder sogar 700 ng/ml. Es ist jedoch mit IGF-1 verbunden, das nach und nach vom IGF-1-Komplex IGFBP freigesetzt wird und nicht mit der gleichen Stärke wie ein separates Protein wirkt und eine anabole Wirkung hat. Das Produkt wirkt schnell und kraftvoll und seine spezifische Wirksamkeit ist viel höher als die des IGF-1-Komplexes: IGFBP, was Sie in Blutuntersuchungen bei der Verwendung von Wachstumshormonen sehen können. Das ist laut der Blutuntersuchung auf Somatomedin C, die Sie im Labor durchführen, der Grund. Es ist sehr schwierig, die Wirksamkeit des Arzneimittels zu bestimmen. In den meisten Fällen wird das frei injizierte IGF-1 im Labor nicht nachgewiesen. Stattdessen sehen Sie die Ergebnisse des IGF-1-Komplexes: IGFBP, der kein klares Bild des tatsächlichen Anstiegs von IGF-1 R potenziellen Risiken bei Peds-Fans vermittelt, es gibt Informationen, die eine Verbindung herstellen IGF-1 mit der Entstehung von Krebs. Obwohl dieser angebliche Zusammenhang große Auswirkungen auf die Massenmedien hat, haben die meisten klinischen und epidemiologischen Zusammenhänge bisher keinen kausalen Zusammenhang zwischen der hormonellen Wachstumstherapie und einem Anstieg des IGF-1-Spiegels sowie einem Anstieg des IGF-1-Spiegels ergeben Krebsrisiko (Werner & amp; Amp; Auf der Grundlage dieser Daten verursacht das IGF-1-Medikament selbst keine Onkologie, hat jedoch nur eine Kontraindikation, wenn Sie bereits an Krebs oder ihre Veranlagung (hohe Krebsmarker) haben. Wachstumshormon und IGF-1 können auch in hohen pharmakologischen Dosen eine bösartige Transformation induzieren. Mit Ausnahme des flüssigen Wachstumshormons) werden gefriert. Wasser) In einer wässrigen Umgebung verschlechtern die Peptide schnell. Dies ist teilweise auf das Vorhandensein von Bakterien zurückzuführen, für die Wasser eine ideale Umgebung für Wachstum und Reproduktion bietet. Das Injektionswasser ist steril. Sobald das Paket jedoch geöffnet ist (normalerweise Ampouel oder Fläschchen), wird die Sterilität beeinträchtigt. Um die Sterilität so lange wie möglich aufrechtzuerhalten, wird Benzilalkohol oder Metacresol für ihre starken antibakteriellen Eigenschaften zugegeben. Dieses behandelte Wasser wird als bakteriostatisch bezeichnet, was bedeutet, dass Bakterien in einem “statischen Zustand” bleiben und sich nicht vermehren. Wachstumshormon und andere Peptide in einer bakteriostatischen Umgebung können ihre Stabilität aufrechterhalten und den Abbau für viel mehr Zeit widerstehen. wie man die Lösung vorbereitet
- Füllen Sie die Spritze mit Wasser. Im Allgemeinen wird der Fläschchengehalt in einem Milliliter Wasser gelöst.
- Wasser in das Fläschchen mit dem gefrier -drossenden Pulver hinzufügen. Kippen Sie die Durchstechflasche so, dass die Nadel die Wand der Durchstechflasche berührt.
- vermeidet es, den dünneren getrockneten Pulver direkt in Kontakt zu treten. Der Dünner sollte langsam entlang der Seiten des Fläschchens fließen (gießen Sie nicht alles auf und vermeiden Sie es zu laufen).
- Sobald das gesamte Lösungsmittel zum Fläschchen mit dem Peptid hinzugefügt wurde, turbine (aber nicht schüttelt) das Fläschchen, bis der gefriergesteuerte Staub gelöst und eine leichte Flüssigkeit erhalten wird. Die Lösung ist nun verwendet.
- Die bei einer Temperatur von 2-8 ° C hergestellte Lösung speichern.
N Siringhe für die Injektion  Wir empfehlen, Spritzen nur aus dem Paket zu verwenden, um eine Infektion zu verhindern (die Wiederverwendung von Spritzen erhöht das Infektionsrisiko). Insulinspritzen werden im Allgemeinen für subkutane Injektionen verwendet und können eine abnehmbare Nadel oder eine feste Nadel haben. Eine der beliebtesten Injektionsnadeln ist der G30. Die Sirings sind normalerweise in 1 ml und 0,5 ml Größe erhältlich. Insulinspritzen sind in U40- und U100 -Formaten erhältlich, die dem Insulingehalt von 40 Einheiten pro 1 ml bzw. 100 Einheiten pro 1 ml entsprechen. Jede Spritze ist speziell für eine bestimmte Art von Insulin ausgelegt. Dies gilt jedoch nicht für die Wachstumshormoneinheiten oder Peptide Mg, daher können beide Spritzen mit angemessenen Anpassungen verwendet werden, um die korrekte Dosierung zu bestimmen. Diese Spritzen haben unterschiedliche Anzeichen und beziehen sich auf diese Anzeichen. Es ist möglich, die Anzahl der Einheiten des zu injizierten Wachstumshormons zu bestimmen. Im Folgenden bieten wir ein Bild an, das die Dosierung verschiedener Peptide zeigt, wenn sie mit 1 ml Wasser für Siringhe U100 und U40 gemischt werden.
Wir empfehlen, Spritzen nur aus dem Paket zu verwenden, um eine Infektion zu verhindern (die Wiederverwendung von Spritzen erhöht das Infektionsrisiko). Insulinspritzen werden im Allgemeinen für subkutane Injektionen verwendet und können eine abnehmbare Nadel oder eine feste Nadel haben. Eine der beliebtesten Injektionsnadeln ist der G30. Die Sirings sind normalerweise in 1 ml und 0,5 ml Größe erhältlich. Insulinspritzen sind in U40- und U100 -Formaten erhältlich, die dem Insulingehalt von 40 Einheiten pro 1 ml bzw. 100 Einheiten pro 1 ml entsprechen. Jede Spritze ist speziell für eine bestimmte Art von Insulin ausgelegt. Dies gilt jedoch nicht für die Wachstumshormoneinheiten oder Peptide Mg, daher können beide Spritzen mit angemessenen Anpassungen verwendet werden, um die korrekte Dosierung zu bestimmen. Diese Spritzen haben unterschiedliche Anzeichen und beziehen sich auf diese Anzeichen. Es ist möglich, die Anzahl der Einheiten des zu injizierten Wachstumshormons zu bestimmen. Im Folgenden bieten wir ein Bild an, das die Dosierung verschiedener Peptide zeigt, wenn sie mit 1 ml Wasser für Siringhe U100 und U40 gemischt werden. Subkutane Injektionen Nach dem Verdünnungsgründen des Peptids mit Wasser ist es für den Einsatz bereit. Alle Peptide werden subkutan oder intramuskulär unter Verwendung einer Insulinspritze injiziert. Sie brauchen:
- Alkohol Kerbe
- Insulinspritze
- Flasche mit der vorbereiteten Lösung
Injektionsverfahren:
- Entfernen Sie die Flaschenkappe.
- die Flaschenkautschukkappe mit Alkohol pleite.
- Nehmen Sie eine Insulinspritze und setzen Sie sie in die Flasche.
- Zeichnet die erforderliche Lösungmenge in der Spritze.
- die Injektionsstelle mit einem Alkoholabstrich reinigen.
- Halten Sie die Nadel mit einem Winkel von 30 bis 45 Grad und Injektion.
- injizieren Sie die Lösung langsam.
- Halten Sie nach Abschluss die Nadel 10 Sekunden lang an Ort und Stelle, bevor Sie sie entfernen, um Lecks der injizierten Flüssigkeit zu vermeiden.
<strong>Speicher </strong> Die korrekte Erhaltung von Peptidmedikamenten ist wichtig, um ihre Wirksamkeit aufrechtzuerhalten. Im Folgenden finden Sie die Richtlinien für die Lagerung von Peptiden in verschiedenen Formen. Lagerung der Form von Staub Die Form von Staub (nicht gemischt) kann bei Raumtemperatur oder im Kühlschrank gespeichert werden. Das gefriergesteuerte Pulver muss von direktem Sonnenlicht und übermäßiger Hitze ferngehalten werden. Unter geeigneten Erhaltungsbedingungen können Peptide in trockener Form maximal 3 Jahre bis 2-8 ° C und bis zu 2 Jahre bei 15 bis 30 ° C gehalten werden Zersetzt sich schnell aus dem Kühlschrank und hält innerhalb von zwei Wochen nur etwa die Hälfte seiner Konzentration. Wenn die Integrität der Verpackung ungewiss ist, ist es daher besser, das Peptid im Kühlschrank zu halten. Lagerung von bakteriostatischem Wasser bakteriostatisches Wasser muss immer im Kühlschrank bei 2-8 ° C gelagert werden, um seine eigene Eigenschaft aufrechtzuerhalten. Wenn das Peptid und das bakteriostatische Wasser zusammengehalten werden, halten Sie den gesamten Kühlschrank. Gedächtnis der Lösung Nach dem Mischen des Staubes mit Wasser vom Ampouel muss die Peptidlösung im Kühlschrank gehalten werden. Ohne Kühlung beginnt sich das Peptid zu verschlechtern und in wenigen Tagen brechen die Moleküle vollständig. Die Speicherdauer für jede Sorte variiert. Zum Beispiel kann Wachstumshormon nur 2-3 Tage im Kühlschrank gehalten werden, während der HCG etwa 5 Wochen dauern kann. Im Durchschnitt können andere Peptide mindestens 30 Tage lang aufbewahrt werden, obwohl einige noch länger dauern können. Die Abbaurate hängt auch von der Anzahl der Bakterien ab, die bei der Durchführung des Fläschchens eingeführt wurden, was bis zu einem gewissen Grad unvermeidlich ist. !!! Halten Sie niemals Peptide im Gefrierschrank !!! Verwendungszwecke mit anabolen Steroiden Es ist auch perfekt geeignet, IGF-1 mit anabolen Steroiden und anderen Arzneimitteln mit ähnlichen Wirkungen zu verwenden. IGF-1-1 verbessert die Auswirkungen von anabolischen Steroiden, indem die Anzahl der Androgenrezeptoren erhöht wird. Das IGF-1-Medikament ist ein äußerst mächtiger Anabolic, der in Kombination mit AS einen sehr großen Anstieg der mageren Muskelmasse verleiht. Gleichzeitig hat IGF -1 viele andere nützliche Eigenschaften, die zusammen den maximalen Hintergrund für das Wachstum erzeugen. Alle anabolen Steroide wirken durch spezielle Strukturen – Rezeptoren auf die Muskeln. Es besteht die Meinung, dass die Anzahl dieser Rezeptoren, wenn Sie für lange Zeit Steroide verwenden, abnimmt. Die Anzahl dieser Rezeptoren nimmt auch mit dem Alter ab. In diesem Fall ist es notwendig, große Dosen von Steroiden zu verwenden. In 20 Jahren handeln 300 mg Testosteronpropionat stärker als 30 Jahre. Bei 30 werden 600 mg für denselben Effekt benötigt. Das IGF-1 aktiviert die Zellen und erhöht die Anzahl der Androgenrezeptoren, und bei 30 wird 300 mg Testosteronpropionat auf die gleiche Weise von 20 Jahren wirken.
Effekte
- Synergistischer Anstieg der Muskelmasse
- synergistischer Effekt der Fettverbrennung
- stärkt die Wirkung von anabolen Steroiden
- Synergistische Wirkung auf die Stärkung von Knochengewebe
Mit dem Wachstumshormon (Somatropin) kann die Verwendung von Somatotropin gleichzeitig ratsam sein, auch wenn es auf den ersten Blick nicht logisch erscheint, aber viele professionelle Bodybuilder tun dies. Wenn sie zusammen verwendet werden, summieren sich ihre Effekte – als anabolischer Effekt für das Muskelwachstum sowie für die Wiederherstellung und Regeneration von Knorpel und anderen Kollagenstrukturen. Darüber hinaus wird das Wachstumshormon und das IGF-1 zusammen die Verbrennung von Fetten erhöhen. Es wurde beachtet, dass zusätzlich zu den vorteilhaften Effekten auch Nebenwirkungen auftreten können. Es ist zu verstehen, dass der IGF -Grad bei beiden Arzneimitteln erheblich zunimmt, sodass diese Verwendung nicht verlängert werden sollte. Effekte
- Synergistischer Anstieg der Muskelmasse
- synergistischer Effekt der Fettverbrennung
- synergistischer Effekt auf die Sehnenreparatur
- Synergistische Wirkung auf die Stärkung von Knochengewebe
- Erhöhung des Risikos von Nebenwirkungen von übermäßigen IGF-1
Verwendungszwecke mit Insulin , wie der Name IGF-1 hervorgeht, hat eine ähnliche Struktur wie Insulin und bindet nicht nur an seinen IGF1R-Rezeptor, sondern auch an den Insulin-und umgekehrt um den Rezeptor. Die Affinität der Bindung zu IGF1R bzw. des Insulinrezeptors ist jedoch unterschiedlich, mit einer hohen Affinität von IGF-1 für IGF1R und etwa eine zehnfache geringere Affinität für den Insulinrezeptor. Die Affinität von Insulin zu seinem Rezeptor ist etwa 100 -mal höher als IGF1R. Trotz der Ähnlichkeit in der Struktur zeigen IGF-1 und Insulin eine andere Verteilung in den Geweben, eine andere Internalisierungskinetik und eine andere subzelluläre Verteilung hormoneller Rezeptoren. Infolgedessen können beide Hormone ähnliche Pfade beeinflussen, jedoch in unterschiedlichem Maße und darüber hinaus andere Wege im Tal aktivieren. Diese Hormone können in der Ebene der Wirkung auf den Glukosestoffwechsel im Körper verglichen werden. Wenn zusammen verwendet wird, wird ein Nebeneffekt wie eine Hypoglykämie (ein Abfall des Zuckerspiegels) ausgesprochen, dass sie Risiken für das Leben verursacht.
Effekte
| Zeit (Wochen) | tägliche Dosierung von IGF-1 LR3 | 1-6 | 20-100 MCG (Betrachten Sie den Start mit einer niedrigeren Dosis zur Bewertung der Toleranz) | 7-12 | weit verbreitet | 13-18 | 20-100 mcg | 19-24 | weit verbreitet |
|---|









Reviews
There are no reviews yet.